Этот заголовок является медицинским определением одной из характеристик иммунной системы человека. Далее по тексту будут раскрыты причины и следствия этого природного феномена, объективно существующего в каждом из читающих эти строки. Статья написана практически в классической манере для публикации в научном издании и неподготовленному читателю будет сложно воспринимать информацию, изобилующей медицинской терминологией и понятиями. Однако вопрос крайне серьёзный и имеет под собой ещё более серьёзные выводы с практическим их применением. В этой связи, статья намеренно не упрощена и не снабжена иллюстрациями. Все пояснения, на любые закономерно возникающие вопросы, будут даны в обсуждениях под текстом.
Сложившиеся еще в XIX в. представления об иммунитете построены на законе Дженнера–Пастера, предполагающем, что первый контакт с патогенным микроорганизмом вызывает у организма иммунитет, проявляющийся при повторных контактах с этим же патогенном. Объяснения иммунных ответов на антиген обычно следуют из правила Бернета, которое утверждает, что антигены рекрутируют специфические лимфоциты из уже существующего репертуара таких клеток и индуцируют их пролиферацию и дифференциацию в эффекторные клетки.
Сегодня в научной литературе накоплены данные о более сложных механизмах взаимодействия иммунной системы человека с патогенными микроорганизмами, чем те, что обычно приводятся в учебных пособиях и даже руководствах для врачей. Было выявлено одно невероятное свойство нашей иммунной системы - при повторном контакте с патогенным микроорганизмом или антигенами, включенными в состав вакцины, различия между старым вариантом эпитопа антигена, и его новым вариантом, зачастую оказывались «незамеченными» иммунной системой. Этот феномен получил название «первичного антигенного греха» и пока не стал объектом пристального исследования отечественных ученых, однако он широко изучается западной школой вирусологии, которые уже выяснили, что в течение всей жизни человека иммунитет будет отвечать на тот антиген, который он запомнил первым.
«Антигенный грех, или антигенный импринтинг, развивается в отношении возбудителей инфекционных болезней, содержащих множество поверхностных эпитопов разной перекрестной специфичности, включающих доминантные эпитопы, перекрестно реагирующие с антителами к антигенам таксономически малосвязанных возбудителей инфекционных болезней или имеющих незначительные отличия в пределах вида. Феномен наблюдается при взаимодействии иммунной системы с антигенно-дрейфующими микроорганизмами (ВИЧ, вирусы гриппа, коронавирусы и т.п.) и микроорганизмами более стабильных видов, но циркулирующих конкурентно как множество разных серотипов и штаммов (лихорадки Денге, малярийные плазмодии и др.). Он также предопределяет тяжесть течения болезни и структуру заболеваемости населения во время эпидемий (пандемий). Осложнения после вакцинации, связанные с антигенным импринтингом, могут проявляться через десятилетия после проведения вакцинации. Вакцинация одной и той же вакциной может дать противоположные результаты в группах населения, имеющих разную эпидемическую историю и ранее многократно вакцинированных вакцинами различающегося антигенного состава.
Феномен впервые четко описан в 1953 г. Davenport et al., обнаружившими низкие титры антител к вирусу серотипа А (H1N1)1 в сыворотке крови людей старше 28 лет и переболевших гриппом до проводимых в начале 1950-х гг. массовых вакцинаций и вакцинированных вакциной на основе вируса этого же серотипа. Однако к вирусу, циркулировавшему ранее, титры антител были неожиданно высокими. Наибольшее количество таких людей приходилось на возрастную группу 35–38 лет, пережившую пандемию гриппа «испанка» в 1918 г. Аналогичные результаты были получены в отношении вируса гриппа серотипа B и его антигенных вариантов. Для объяснения иммунологического феномена Davenport et al. предположили, что во время первого инфицирования вирусом гриппа еще в детском возрасте, иммунная система ориентируется на некий доминантный антиген среди циркулирующих штаммов вируса. Последующее контакт с вирусами гриппа, антигенносвязанными с предыдущим, вызывает подъем уровня антител не на их антигены, а на штамм, вызвавший первую инфекцию. Это наблюдение было кратко резюмировано в виде «доктрины первичного антигенного греха» («the doctrine of original antigenic sin»).
Первичный Антигенный Грех: Как Детские Инфекции Могут Формировать Пандемии
Первая инфекция гриппа, перенесённая в детстве, формирует иммунитет к будущим вирусам гриппа, включая новые пандемические штаммы, передаваемым воздушно—капельным путем,. Но не все штаммы гриппа стимулируют одинаковую начальную иммунную защиту, согласно новым данным, опубликованным сегодня вирусологами Школы медицины Питтсбургского университета в журнале PLOSPathogens.
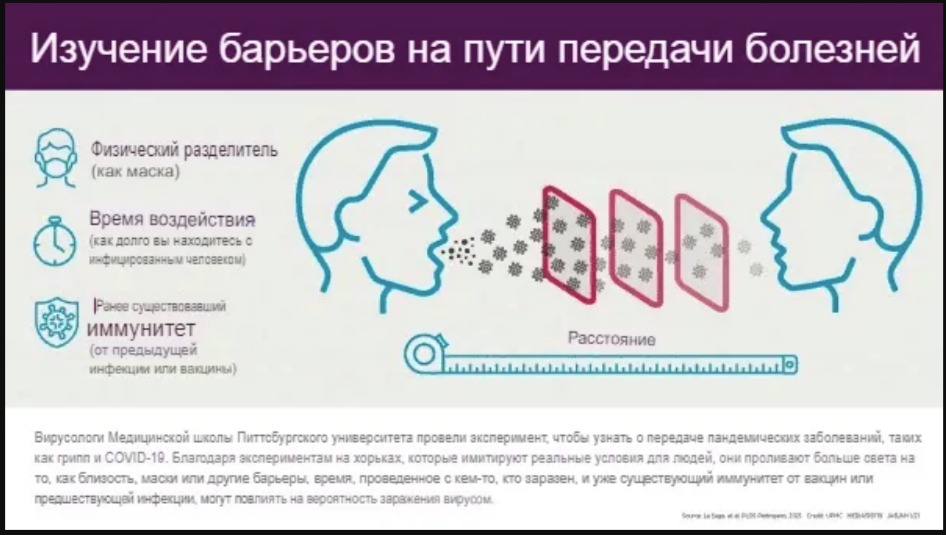
“Эти результаты имеют отношение прямо сейчас к пандемии COVID-19”, - сказала старший исследователь Сима Лакдавала, PhD философии, доцент микробиологии и молекулярной генетики в Питте. “Они могут объяснить распределение тяжести и восприимчивости к SARS-CoV-2 по возрасту.
“Перенесённый впервые грипп, не делает человека невосприимчивым ко всем будущим вирусам гриппа”, - сказала она. “Кроме того, присутствие оригинального вируса SARS в 2003 году или любого из коронавирусов, вызывающих "обычную простуду" не обязательно означает, что вы не можете заразиться SARS-CoV-2. Но ваша восприимчивость к инфекции может отличаться от восприимчивости человека, который никогда не сталкивался с коронавирусом”.
Лакдавала и ее коллеги разработали эксперимент с использованием хорьков, которые, как показали предыдущие исследования, обладают такой же восприимчивостью и иммунной реакцией на грипп, как и люди, и имитировали реальные человеческие условия. Эксперимент был разработан для проверки концепции “Первичного антигенного греха”, когда первое воздействие патогена на человека накладывает отпечаток на его иммунитет ко всем будущим родственным инфекциям.
Это явление наблюдается у населения, пострадавшего от предыдущих эпидемий и пандемий гриппа. Например, пандемия гриппа H1N1 2009 года непропорционально сильно затронула людей в возрасте от 5 до 24 лет, что свидетельствует о том, что пожилые люди подвергались воздействию предыдущего штамма гриппа, который давал им стойкий иммунитет, защищая их от нового штамма.
В эксперименте с хорьками ученые заразили разные группы хорьков, которые никогда не болели гриппом, одним из двух разных штаммов гриппа — сезонным гриппом H3N2 или пандемическим гриппом H1N1 2009 года — и подождали три месяца, чтобы иммунная система успокоилась и выработала более зрелый иммунитет к любому штамму, которому они подвергались.
Затем хорьки с иммунитетом к H3N2 подвергались воздействию хорьков, зараженных вирусом H1N1, а хорьки с иммунитетом к H1N1 подвергались воздействию хорьков, зараженных вирусом H3N2.
Ученые имитировали человеческие рабочие и выходные дни, моделируя общение зараженных хорьков со своими товарищами по 8 часов в день в течение пяти дней - примерно так, как люди, пересекались бы, работая в замкнутых пространствах, или непрерывно контактируя в течение двух дней, подобно семейным выходным.
Хорьки с предыдущей инфекцией H1N1 имели защиту от воздушно-капельной передачи гриппа H3N2 от заразного товарища. Но хорьки с предыдущей инфекцией H3N2 не имели такого же уровня защиты от H1N1 и заражались с той же скоростью, что и животные без предварительного иммунитета.
“Это было действительно удивительно", - сказала Лакдавала. “Наш иммунитет может определять, насколько мы восприимчивы к последующим инфекциям, но это происходит не на регулярной основе. Мы долгое время игнорировали тот факт, что не каждый штамм вируса будет передаваться в популяции одинаково. Это важно понимать при подготовке к будущим пандемиям”.
Эксперимент не показал, почему хорьки с предыдущей инфекцией H1N1 были защищены от H3N2, ни почему предыдущая инфекция H3N2 не блокировала H1N1. Но ученые обнаружили, что иммунитет не был обусловлен нейтрализующими антителами, которые являются антителами, приобретенными после вакцинации или инфекции, которые специально нацелены и нейтрализуют определенный патоген. Это открытие указывает на то, что иммунитет, вероятно, был обусловлен адаптивным иммунным ответом—это означает, что предыдущая инфекция H1N1 заставила иммунную систему следить за H3N2 и быстро устранить его.
Необходимы будущие исследования, чтобы выявить точный иммунологический механизм, лежащий в основе такого иммунного ответа. Но Лакдавала сказала, что это не означает, что органы общественного здравоохранения должны ждать, чтобы применить полученные результаты в действии, особенно в разгар пандемии COVID-19. Понимание различных способов воздействия инфекций на людей, основанных на предыдущем воздействии, может быть использовано для целевых мероприятий или программ вакцинации, основанных на возрасте.
Прошлые встречи с вакциной против гриппа формируют реакцию на вакцину
Изученные случаи гриппа и эффективность вакцины против гриппа
Иммунная история влияет на эффективность вакцины, взаимодействуя с другими потенциальными проблемами, возникающими в процессе производства.
Низкую эффективность вакцины против гриппа часто связывают с проблемами самой разработки и производства вакцин. Иногда штаммы гриппа, выбранные для вакцины, плохо соответствуют тем, которые циркулируют среди населения, особенно в те годы, когда преобладает штамм H3N2. Большинство вакцин против гриппа, получаемых в мире, выращиваются в куриных яйцах, что может привести к мутации и отличию вируса от циркулирующих штаммов и, таким образом, что сделает вакцину менее защищающей.
В 2012-13 годах компонент H3N2 вакцины против гриппа был эффективен только у 39 процентов людей. В этом сезоне должностные лица общественного здравоохранения считали, что использование яичных эмбрионов, является проблемой. Но в новом исследовании, опубликованном на этой неделе в журнале Clinical Infectious Diseases, исследователи из Университета Чикаго, Гарвардского университета и другие показывают, что плохие иммунные реакции, а не выращивание вируса в куриных эмбрионах, могут объяснить низкую эффективность вакцины в этом году.
«Использование яичных эмбрионов имеет переменный успех, - говорит Сара Коби, доцент кафедры экологии и эволюции в Чикаго и ведущий автор исследования. «Иногда они имеют значение, а иногда и нет, но то, что, по-видимому, имеет наибольшее значение, - это иммунная история».
То, что имеет значение, похоже, является феноменом, известным как «первичный антигенный грех». Вакцины против гриппа предназначены для того, чтобы иммунная система могла продуцировать антитела, которые распознают специфические штаммы вируса, с которым кто-то может столкнуться в конкретном году. Эти антитела нацелены на уникальные участки вируса H3N2 и блокируют их, чтобы отключить его. Как только иммунная система уже имеет антитела для нацеливания на данный участок вируса, она предпочтительно повторно активирует одни и те же иммунные клетки при последующем заражении вирусом.
Это эффективно для иммунной системы, но проблема в том, что вирус из-за этого меняется из года в год. Участок, который распознает антитела, все еще может быть там, но уже не может быть решающим для нейтрализации вируса. Антитела, полученные из наших первых встреч с гриппом - либо из вакцин, либо из-за инфекции - имеют тенденцию преобладать над теми, которые были получены в результате последующих прививок. Таким образом, даже если вакцина хорошо подходит для данного года, если у кого-то есть история взаимодействия с гриппом, иммунный ответ на новую вакцину может быть менее эффективным, поскольку вакцина может вызывать слабый иммунный ответ у многих, кто её получает.
«Мы видим, что как вакцинированные, так и невакцинированные люди были инфицированы подобными вирусами гриппа и что вакцина не вызывала сильного иммунного ответа у большинства людей в нашем исследовании», - сказал Йонатан Град, PhD медицинских наук, доцент иммунологии и инфекционных заболеваний в Harvard TH Чан из школы общественного здравоохранения и являющийся соавтором исследования.
Исследователи часто проверяют взаимосвязь между разными штаммами гриппа и тем, насколько хорошо инфекция/ вакцинация против одного штамма защищает вас от заболевания другим, на лабораторных животных, таких как хорьки. В 2012-13 годах хорьки, иммунизированные выращенным на яичных эмбрионах штаммом, вырабатывали антитела, которые плохо реагировали с циркулирующими в том сезоне штаммами H3N2. Поэтому ученые положили, что всему виной было использование яичных эмбрионов. Но когда Коби, Град и их коллеги проанализировали образцы крови у людей, которые были вакцинированы в том году, они не обнаружили различий в ответах на антитела к вакцине или циркулирующим штаммам. Похоже, что их иммунная система не удосужилась распознать различия в отношении мутаций, потому что они уже признали так много других участков вакцинного штамма.
«Представьте, что вирусы гриппа похожи на разные марки и модели автомобилей, - сказал Град. «Хорьки, которые раньше не видели гриппа, научились рассказывать о разнице между тесно связанными штаммами, например, рассказывая о различии между Honda Civic и Toyota Camry. Но люди не различали их, а вместо этого просто видели машины».
Это не значит, что использование яичных эмбрионов для выращивания штаммов не всегда имеет значение. В отдельном исследовании, проведенном в 2017 году, Коби и команда, возглавляемая исследователями из Университета Пенсильвании, обнаружили, что использование яичных эмбрионов привело к несоответствиям в наиболее распространенной вакцине, полученной в 2016-17 гг., ещё в одном сезоне, в котором доминировал H3N2.
Использование яичных эмбрионов может быть фактором во время рекордного сезона гриппа в этом году. H3N2 снова является преобладающим штаммом, из-за которого люди болеют, а самая распространенная вакцина такая же, как и в прошлом году, с ее потенциально проблематичным использованием яичных эмбрионов.
Однако есть альтернатива. Новые вакцины, выращенные без яиц, либо в клетках насекомых, либо в клетках почек собак, гораздо менее склонны к развитию мутаций, которые могут сделать их менее эффективными против гриппа. До сих пор они были более дорогими, но исследователи надеются, что продолжение исследований поможет перенести внимание на эти более эффективные вакцины.
«Не было достаточного потребительского и медицинского спроса для перехода на более эффективные вакцины», - сказал Коби. «До недавнего времени также не проводилось столько исследований по сложности и вариациям иммунного ответа на грипп».
«Нам нужно сделать более фундаментальные исследования о том, как стимулировать ответы на нужные участки вируса, и это потребует от нас понимания первичного антигенного греха лучше», - сказала она. «Нам также необходимо понять, почему вакцина, по-видимому, плохо срабатывает в некоторых случаях у некоторых людей в определённое время. На самом деле нет ответа, или мы просто смотрим не туда?»
Исследование «Бедная иммуногенность, а не использование яичных эмбрионов в производстве вакцины, может объяснить низкую эффективность вакцины против гриппа H3N2 в 2012-13 годах», был поддержан Национальным институтом аллергии и инфекционных заболеваний, Фондом Wellwell Burroughs, Фондом семьи Смитов и Дорис Дюк Благотворительный фонд.
Иммунолог Wistar Скотт Хенсли Прокомментировал отчет CDC о вакцине против гриппа у пожилых людей
В отчете, опубликованном в четверг Центрами по контролю и профилактике заболеваний, описано, как вакцина против сезонного гриппа в этом году была эффективна только на девять процентов для защиты людей в возрасте 65 лет и старше от штамма гриппа, который в настоящее время циркулирует. (Как видно из этой статьи Ассошиэйтед Пресс).
Иммунолог Wistar Скотт Хенсли, PhD философии, изучающий грипп, поделился информацией о новостях CDC:
“Неизвестно, почему вакцина этого года оказалась неэффективной среди пожилого населения. Мы знаем, что иммунная система пожилых людей в целом работает хуже, чем у молодых людей. Существуют различные дефекты в иммунном ответе пожилых людей, поэтому мы можем только гадать, почему пожилые люди плохо реагируют на вакцину этого года.
“В 1950-х годах было отмечено, что люди склонны усиливать антителозависимые реакции против ранее циркулировавших штаммов гриппа за очевидный счет усиления антителозависимых реакций против новых антигенно отличных вирусных штаммов. В настоящее время мы исследуем, произошел ли этот процесс, называемый "первичным антигенным грехом", у пожилых людей, получивших вакцину против гриппа в этом году. Несмотря на то, что вакцина этого года не особенно хорошо подействовала на пожилых людей, стоит подчеркнуть, что вакцины против гриппа по-прежнему являются лучшей защитой от гриппа.
Хенсли изучает грипп и явления “антигенного дрейфа”, то есть то, как мутации изменяют поверхностные молекулы вируса гриппа с течением времени. Вакцины позволяют иммунной системе вырабатывать антитела против этих поверхностных молекул (называемых “антигенами”), однако мутации в этих молекулах позволяют постоянно появляться новым штаммам гриппа, устойчивым к вакцинам. Антигенный дрейф-это то, что требует от ученых ежегодно разрабатывать новую прививку от гриппа.
Вирусолог Надежда Жолобак: Почему коронавирус не эффективен как оружие и куда исчезают антитела?
с 26:30 до 30:31
Именно первичный антигенный грех является причиной антителозависимого усиления инфекционного процесса. Потому что эти антитела не нейтрализуют полноценно этот вирус, а наоборот способствуют его распространению.
И тут снова я возвращаюсь к прививкам. Если мы прививаем против короновируса, прививка очень сильная, так. И она провоцирует формирование антител именно против вот этого штамма короновируса. То изменение штамма короновируса, а мы понимаем, что изменение будет, он же изменяется так же как грипп, чуть-чуть медленнее в два раза, то соответственно люди, привитые против этого предыдущего штамма, при контакте с новым не будут формировать нормальных антител. Они будут более слабыми и соответственно развитие инфекции, развитие инфекционного процесса может быть более тяжелым, если бы они были не привиты.
Это так называемое слепое пятно иммунной системы. Оно не видит этих различий штаммовых, при том при всём, что они есть. И в результате эти антитела не нейтрализуют вирус. Об этом тоже нужно помнить перед тем, как запускать этот иммунный процесс гиперактивации нашей иммунной системы.
5:50 – 9:32 Развитие антителотоксичной зависимости на примере вакцины от вируса Денге четырёхвалентной (против 4-х разных штаммов), которая усиливает течение болезни и о SARS-COV-2.
Дело в том, что эта история на слуху и по поводу коронавирусов и по поводу таких очень известных вирусов. Это и вирус Эбола и вирус Денге.
Кстати с вирусом Денге очень такая неприятная история. Сделана была вакцина против вируса Денге, против четырёх различных вариантов вируса Денге. И вот введение такой вакцины детям, которые не контактировали с вирусом Денге, существенно (это статистически было доказано) отягощает течение самой болезни Денге, когда эти дети контактируют с этим вирусом. И вакцинация такой вакциной была прекращена.
Дело в том, что для коронавируса такие факты были показаны. За этот год, 2020 – 2021, во-первых резко увеличилось количество публикаций. Если вы зайдёте на Википедию и напишите «антителозависимая клеточная цитотоксичность» на английском языке, то там выпадет статья огромнейшего размера, которая описывает развитие именно этого симптома антителозависимой цитотоксичности.
(замечание ведущего - Она же называется цитокиновый шторм) Нет цитокиновый шторм это немножко другое. Дело в том, что цитокиновый шторм связан с продукцией провоспалительных цитокинов, а антителозависимая клеточная токсичность это составляющая клеточного иммунного ответа. То есть наш ответ состоит из двух составляющих. Это клеточный и гуморальный иммунный ответ. Клеточный иммунный ответ это активация клеток, которые уничтожают вирус инфицированные клетки, а гуморальный иммунный ответ (гумурос в переводе жидкость) это антитела, это цитокины, различные, которые продуцируются в организме в ответ на контакт с возбудителем. Не обязательно с вирусом. Это может быть бактериальный ответ точно так же. Но для вирусной инфекции показана продукция определённых провоспалительных цитокинов, которые запускают воспалительную реакцию. Без неё мы бы не удалили вирус. Она нужна.
Но она нужна в определённых пределах. И вот цитокиновый шторм это как раз активация гуморального ответа. А антитело зависимая цитотоксичность это активация клеточного иммунного ответа, когда происходит самоуничтожение собственных клеток. И в данной ситуации, именно антитело зависимая цитотоксичность, это характерно и для коронавирусов, и для вирусов гриппа это тоже показано. То есть, когда мы имеем неполноценные антитела, которые не могут полностью нейтрализовать вирус, то последующий контакт с таким возбудителем приводит к тому, что у нас отягощается течение заболевания.
Кстати в своё время пытались разработать, и до сих пор не разработали адекватные вакцины против коронавирусов у кошек, например. Кошек прививают этими вакцинами, а потом кошки дохнут, когда контактируют с коронавирусом диким. Поэтому разработка таких вакцин это достаточно сложный путь. И гарантировать, что в каждом случае на фоне прививания сформируются полноценные антитела, которые реально будут нейтрализовать вирус и не будут запускать активацию этого клеточного ответа никто не может дать.
Поэтому вообще запуск синтеза антител и активного синтеза антител, это в общем-то, не всегда является хорошим прогностическим результатом.
Теперь вы знаете мнение профессионалов, скрупулёзно изучивших описанную выше проблему и возможные последствия вакцинации. Ещё раз уточню, что разработка вакцины для людей от SARSCOV-19 обошлась БЕЗ доклинических испытаний. Иными словами, ни одна кошка и ни один хорёк не пострадали. Теперь решение за вами, не говорите потом, что вы были не информированы или дезинформированы.
P.S. Данная статья написана в соавторстве с Tate Untold, за что выражаю ей глубокую признательность и уважение. )















Оценили 62 человека
111 кармы